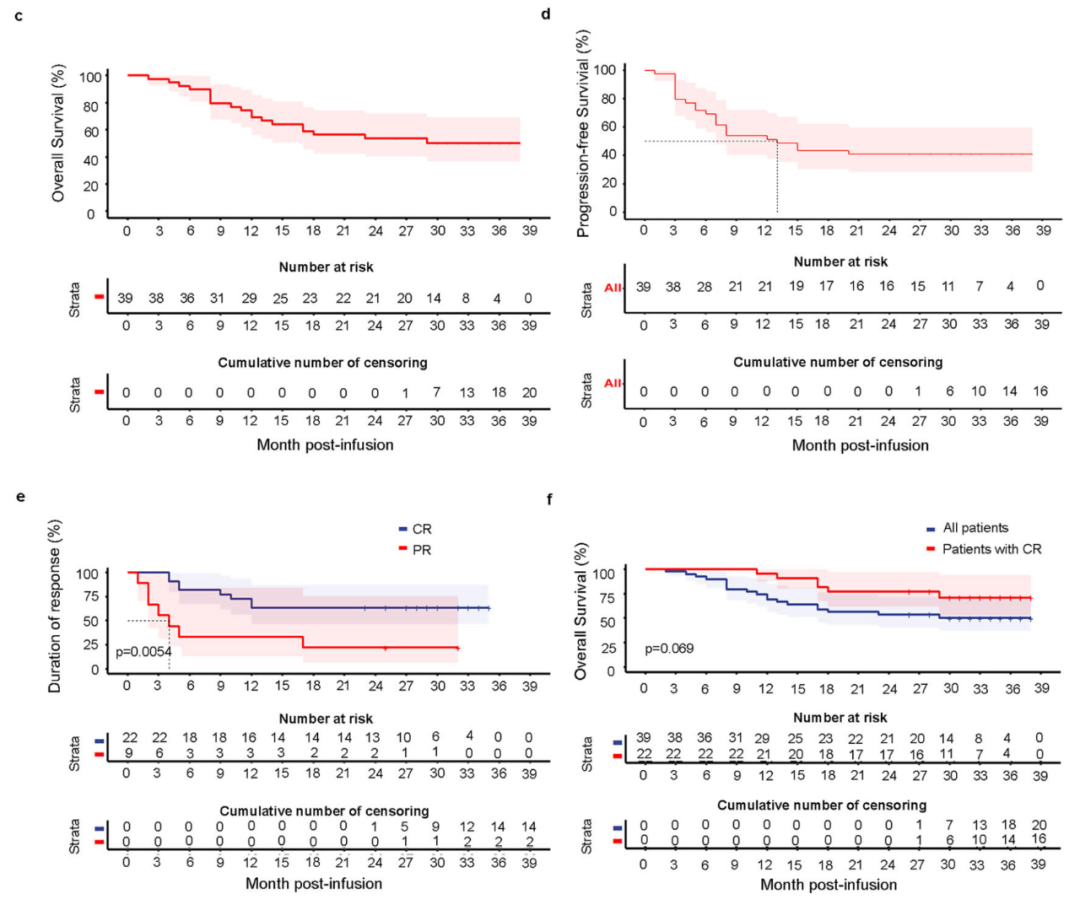
CAR-T细胞疗法在血液系统恶性肿瘤领域取得了里程碑式突破,迄今为止,美国FDA已批准了六种CAR-T细胞疗法上市。抗CD19 CAR-T细胞疗法有可能成为淋巴瘤患者的治愈性疗法。然而,大多数患者要么对治疗无效,要么在初步缓解后再次复发。为了提高CAR-T细胞疗法的效果,许多创新的CAR设计已经被开发出来,以增强抗肿瘤效率,克服与CAR-T细胞扩增、浸润和持久性不足相关的治疗耐药性。在这方面,第四代CAR(装甲型CAR)正在开发中,它结合了细胞因子(IL-7、IL-15或IL-21等),以提高CAR-T细胞的持久性、肿瘤靶向性和抗肿瘤能力。另一种策略是通过表达趋化因子受体或趋化因子(CCL19、CCL21)来修饰CAR-T细胞,引导CAR-T细胞到达肿瘤部位。这些策略的可行性已经在临床前研究中得到了证明,并在一系列恶性肿瘤的临床试验中进行了评估。近年来,表达IL-7和CCL19的抗CD20 CAR-T细胞显示出更强的抗肿瘤活性,并在小鼠模型体内实现了对实体瘤的完全清除。尽管在不同实体瘤模型中的临床前证据支持了装甲型CAR-T策略的潜在抗肿瘤疗效,但缺乏在人类中的临床结果。2024年1月9日,浙江大学医学院第一附属医院钱文斌教授、温州医科大学高基民教授、张劲翼研究员等在 Cell Discovery 期刊发表了题为:Safety and feasibility of anti-CD19 CAR T cells expressing inducible IL-7 and CCL19 in patients with relapsed or refractory large B-cell lymphoma 的研究论文。该研究报告了共表达IL-7和CCL19(7×19)的第四代抗CD19 CAR-T细胞疗法在复发/难治性大B细胞淋巴瘤(R/R LBCL)患者中的安全性和有效性,结果显示了该疗法持续效果和可控副作用,支持了7×19 CAR-T细胞作为一种有前途的B细胞恶性肿瘤的治疗策略。该研究开发了一种新型CAR-T细胞疗法——7×19 CAR-T细胞疗法,通过工程化CD19特异性CAR-T细胞,在接触CD19抗原时自分泌IL-7和CCL19。临床前研究确定了7×19 CAR-T的抗淋巴瘤活性,证实其优于传统的抗CD19 CAR-T细胞的肿瘤靶向性和抗肿瘤细胞活性。基于临床前数据,研究团队在成人复发/难治性大B细胞淋巴瘤(R/R LBCL)中进行了一项多中心临床试验,该论文报告了7×19 CAR-T细胞疗法的安全性和有效性。该临床试验显示,在剂量递增阶段,未观察到剂量限制性毒性。39例R/R LBCL患者接受了7×19 CAR-T细胞治疗,剂量范围为0.5×106-4.0×106细胞/kg体重。39例患者中5例(12.8%)发生了3级细胞因子释放综合征,4例(10.3%)患者发生了≥3级神经毒性,这些副作用在治疗后得到完全缓解。7×19 CAR-T细胞单次输注后3个月的总缓解率为79.5%(完全缓解率为56.4%;部分缓解率为23.1%)。中位随访时间为32个月,中位无进展生存期为13个月,中位总生存期尚未达到,2年时的预计生存率为53.8%。 总的来说,这些来自多中心临床研究的长期随访数据表明,在R/R LBCL患者中,7×19 CAR-T细胞疗法可以诱导持久缓解,中位总生存期超过2年,并且具有可管理的安全性。
https://www.nature.com/articles/s41421-023-00625-0
来源 | 生物世界(公众号)