Dev Cell | 王兰团队发现SMARCA5重编程AKR1B1介导的果糖代谢来控制白血病的发生
染色质可及性的显著变化是白血病的表观遗传特征。然而,白血病中这种变异的原因仍然难以捉摸。
2024年5月21日,中国科学院上海营养与健康研究所王兰团队在Developmental Cell 在线发表题为“SMARCA5 reprograms AKR1B1-mediated fructose metabolism to control leukemogenesis”的研究论文,该研究表明SMARCA5重编程AKR1B1介导的果糖代谢来控制白血病的发生。该研究确定了SMARCA5,一个模仿开关(ISWI)染色质重塑复合体的核心ATP酶,是白血病细胞中异常染色质可及性的原因。
该研究发现,在白血病发生过程中,SMARCA5需要维持异常染色质的可及性,然后通过募集转录共激活因子DDX5和转录因子SP1来促进aldo/酮还原酶AKR1B1的转录激活。较高水平的AKR1B1与白血病患者预后不良有关,并通过重编程果糖代谢促进白血病发生。此外,AKR1B1的药理抑制已被证明对白血病小鼠和白血病患者细胞具有显著的治疗作用。因此,该研究结果将SMARCA5介导的异常染色质状态与AKR1B1介导的内源性果糖代谢重编程联系起来,并揭示了AKR1B1在白血病发生中的重要作用,这可能为白血病的治疗提供策略。

白血病是一种侵袭性克隆性血液系统恶性肿瘤,其特征是异常的自我更新和不成熟的造血干细胞/祖细胞(HSPCs)。一些研究揭示了白血病在调控基因转录、染色质状态和DNA修饰方面的基因组和表观遗传学改变,这些改变被认为是白血病干细胞(LSCs)的增加和白血病的发生、进展和复发的原因。尽管在过去的几十年里,急性髓性白血病(AML)的常规化疗取得了进展,但由于复发相关的耐药白血病细胞,AML患者的5年总生存率仍然很低(平均5年总生存率低于30%)。因此,迫切需要探索有针对性的治疗策略。
表观遗传失调在癌症的发生和发展中起着重要作用。越来越多的证据表明,白血病患者中染色质状态和表观遗传调控异常的频率很高,这些异常通过基因表达异常与白血病的发病有关。此外,已经确定不同亚型的白血病具有独特的染色质可及性。与相应的正常造血细胞相比,白血病中染色质可及性的差异随着患者造血干细胞(HSC)向白血病母细胞(LSCs)的进展而增加。然而,导致白血病染色质不可接近变异的染色质调节因子在很大程度上仍然未知。SMARCA5是保守模仿开关(ISWI)染色质重塑复合体的核心ATP酶,负责核小体间距、滑动和射出,并参与几个不同亚基的转录调控。它是DNA双链断裂(DSB)修复和胎儿造血所必需的。然而,在造血系统恶性肿瘤中,SMARCA5的表观遗传功能及其与异常染色质可及性的关系尚不清楚。
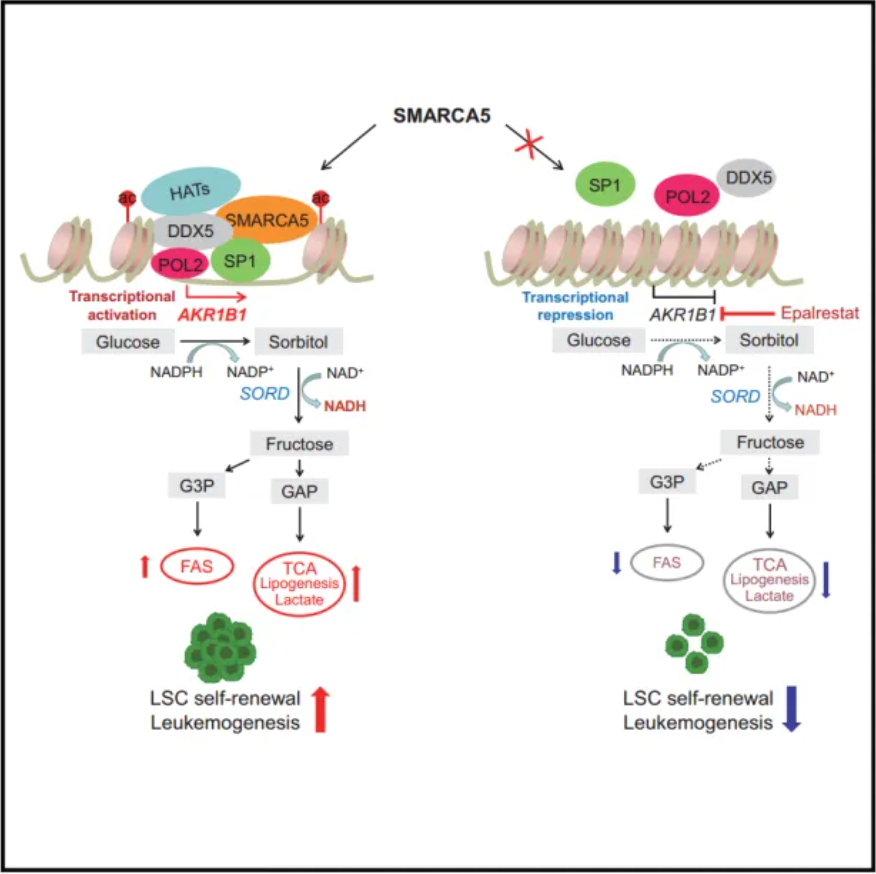
机理模式图(图源自Developmental Cell )
新陈代谢重编程是癌症的一个特征与正常造血干细胞相比,白血病细胞中枢能量代谢的异质性已得到证实。LSCs具有较高的线粒体氧化磷酸化(OXPHOS),靶向OXPHOS可以根除LSCs。最近的研究表明,白血病患者的果糖利用率较高,这在以前是有利于白血病发生的。内源性果糖可以通过多元醇途径从葡萄糖转化而来。然而,内源性果糖代谢是否是白血病发生所必需的,以及白血病发生中的这种重编程代谢状态是否受到异常染色质可及性的控制,目前尚不清楚。
在白血病发生过程中,SMARCA5主要负责维持异常的染色质可及性。这种由SMARCA5介导的异常染色质状态促进了DDX5和转录因子SP1的沉积,从而激活了AKR1B1的转录,从而导致白血病的重编程代谢状态。靶向AKR1B1介导的内源性果糖代谢可能选择性地抑制白血病的进展,且毒性适中。总之,该研究将白血病中染色质可及性的表观遗传失调与内源性果糖代谢重编程联系起来,并发现了一种通过靶向内源性果糖代谢来治疗白血病的有效策略。
原文链接:
https://doi.org/10.1016/j.devcel.2024.04.023
来源 | iNature(公众号)
声明:本网站所有内容来源注明为“新医事”,版权均属于新医学事所有,未经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“新医事”。本网注明来源为其他媒体的内容为转载,或系自媒体发布的内容,仅系出于传递更多信息之目的,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。






