EMM丨中山大学王军舰等团队合作发现重塑细胞外基质是抑制小细胞肺癌转移的潜在治疗靶点
小细胞肺癌(SCLC)是最具侵袭性和致命性的肺癌类型,其特点是治疗选择有限、早期和频繁转移。然而,目前无法明确SCLC发生转移的决定因素。
2024年7月31日,中山大学王军舰、佛山市第一人民医院冯卫能、暨南大学陆小云共同通讯在EMBO Molecular Medicine 在线发表题为“Therapeutic targeting ERRγ suppresses metastasis via extracellular matrix remodeling in small cell lung cancer”的研究论文。该研究发现雌激素相关受体γ(ERRγ)在转移性SCLC肿瘤中过表达,并且与SCLC进展呈正相关。
ERRγ作为细胞外基质(ECM)重塑和细胞粘附(转移中的两个关键步骤)的重要激活剂,直接调节参与这些过程的主要基因表达来发挥作用。对ERRγ的遗传和药理学抑制显著减少胶原蛋白的产生、细胞-基质粘附、微丝的产生,最终阻断SCLC细胞的侵袭和肿瘤转移。值得注意的是,在多细胞来源和患者来源的异种移植模型中,ERRγ拮抗剂显著抑制肿瘤生长和转移,并恢复SCLC对化疗的敏感性。综上所述,该研究确定ERRγ是转移性小细胞肺癌的重要机制靶点,为治疗该疾病提供了一种潜在的药理学策略。

小细胞肺癌(SCLC)是一种高级别神经内分泌癌,约占所有肺癌发生率的15%,是最具侵袭性和致死性的肺癌亚型。与非小细胞肺癌(NSCLC)相比,SCLC的特点是增殖率更高,转移期更早,预后更差。转移是癌症相关死亡的主要原因,大多数SCLC患者被诊断为远端转移。SCLC常见的转移部位包括肝脏、淋巴结、脑和骨骼。SCLC的标准一线治疗包括化疗(顺铂或卡铂联合依托泊苷)联合免疫疗法(程序性细胞死亡蛋白1(PD1)抗体和PD1配体1(PD-L1)抗体)。但由于治疗耐药性,SCLC往往会复发或恶化,中位总生存期(OS)仅为12-15个月。克服耐药性已成为改善SCLC预后的主要障碍和需要解决的核心问题。因此,迫切需要确定新的治疗靶点,并制定更有效的SCLC治疗策略。
核受体超家族由48个关键转录因子组成,是一类共同代表了人类疾病主要治疗药物靶点的蛋白质。这些受体具有保守的配体结合域,是基于配体的药物研发和治疗干预的理想靶点。雌激素相关受体γ(ERRγ,由ESRRG基因编码)与ERRα和ERRβ一起构成核受体亚家族ERR。ERR与雌激素受体(ER)具有高度的序列相似性,但不与内源性雌激素或其衍生物结合。迄今为止,尚未发现ERR的内源性配体,是孤儿核受体亚家族的一员。
与ERRα和ERRβ一样,ERRγ不依赖配体,以二聚体或单体的形式与ERR反应元件(ERRE)结合来发挥其转录活性,ERRγ的转录活性受共激活因子或辅阻遏蛋白的调节。ERRγ在肿瘤中的作用涉及许多生理过程,如耐药性、间充质到上皮的转变和细胞代谢。据报道,ERRγ通过靶向S100A4促进子宫内膜癌细胞的迁移和转移。此外,在肺腺癌A549细胞中,ERRγ有助于双酚A(BPA)诱导的上皮间充质转化(EMT)。然而,尚不清楚ERRγ在SCLC发病机制中的作用。
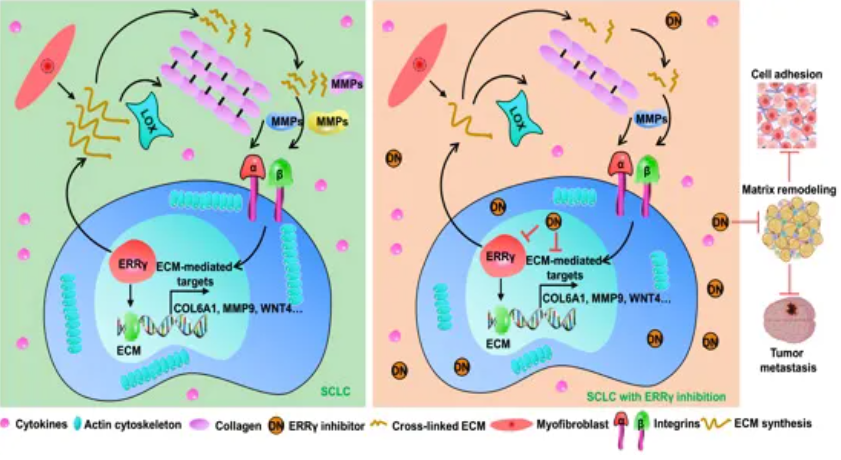
ERRγ在细胞外基质(ECM)重塑过程中发挥着关键作用(摘自EMBO Molecular Medicine )
细胞外基质(ECM)是肿瘤微环境(TME)的非细胞成分,主要由蛋白聚糖、糖蛋白、基质细胞蛋白和结构蛋白组成。以蛋白含量、活性和交联变化为特征的ECM重塑是癌症进展的关键因素。最常见的致癌ECM重塑涉及纤维状胶原蛋白的过度合成和沉积,随着重塑酶的表达,产生支持癌症侵袭和转移的结构和生物活性环境。SCLC被ECM基质包围,通过激活β1整合素来保护癌细胞免受化疗诱导的细胞死亡,从而激活磷酸肌醇-3-OH激酶(PI3-激酶)。整合素β1还可以通过激活下游黏着斑激酶/SRC(FAK/SRC)信号传导来促进SCLC转移。然而,尚不清楚ECM加速SCLC进展的分子机制。
该研究发现ERRγ在SCLC肿瘤中显著过表达,特别是在转移灶的SCLC肿瘤细胞中。ERRγ直接调节相关基因的转录,是细胞外基质(ECM)重塑和细胞粘附的决定因素。ERRγ拮抗剂通过ECM重塑强烈抑制SCLC异种移植物中的肿瘤生长和转移。此外,研究发现ERRγ拮抗剂改善了肿瘤对化疗的耐药性。结果表明,ERRγ可能是晚期SCLC的一个新型治疗靶点。
参考消息:
https://www.embopress.org/doi/full/10.1038/s44321-024-00108-z
来源 | iNature(公众号)
声明:本网站所有内容来源注明为“新医事”,版权均属于新医学事所有,未经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“新医事”。本网注明来源为其他媒体的内容为转载,或系自媒体发布的内容,仅系出于传递更多信息之目的,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。






