冷冻电镜+人工智能+虚拟筛选,加快药物发现速度,Deep Apple获5200万美元A轮融资
近日,著名生命科学风险投资公司 Apple Tree Partners 孵化的新药研发公司 Deep Apple Therapeutics 走出隐身模式,完成5200万美元A轮融资。
Deep Apple 公司的目标是开发一种结合冷冻电镜、深度学习和分子对接筛选的药物发现引擎,该引擎应该能够加速先导化合物的优化(将时间缩短至一年以内),并实现对传统药物发现方法无法实现的生物靶标信号的追踪,从而缩短药物发现时间,提高候选药物在临床和商业上成功的可能性。

Deep Apple的创始首席执行官、Apple Tree Partners 合伙人 Spiros Liras 博士表示,只有1%的临床候选药物来自虚拟筛选,我们认为这不是一个限制,而是一个药物发现的范式转变的重大机遇。
Deep Apple 的药物发现引擎基于其三位学术联合创始人的研究成果:
Georgios Skiniotis 是斯坦福大学分子与细胞生理学和结构生物学教授,是一位世界著名的结构生物学家,一直在推动冷冻电镜的前沿,以研究具有挑战性的生物系统,特别是G蛋白偶联受体(GPCR)的信号机制和药理学。他的实验室开发了一种先进的冷冻电镜平台,作为Deep Apple药物发现引擎的基础成像能力。该平台不仅可以捕捉GPCR的高分辨率结构,还可以捕捉GPCR的动态信息,包括在经验性高通量筛选中可能被忽略的关键中间结构状态,而这可能与药物发现的疾病状态生物学最相关。
Brian Shoichet 和 John Irwin 是加州大学旧金山分校(UCSF)药学院教授,他们是药物发现大型文库对接的先驱,成功地将该技术应用于多个药物靶点,特别是GPCR。他们帮助帮助创建了超过600亿个可合成化合物的大型虚拟文库,并展示了如何通过基于结构的分子对接筛选该文库的子集,以获得有效的配体,其活性通常在纳摩尔范围内。这种技术构成了Deep Apple分子对接方法的基础,并能够在特定项目的基础上创建专有的虚拟文库。
Spiros Liras 博士表示,原始的二维冷冻电镜数据通常会被人眼过滤,导致大部分数据被丢弃。而Deep Apple利用深度学习分析所有原始的二维冷冻电镜数据,以加快高质量三维图像的创建,并从中提取蛋白质构象状态的动态信息,例如它们是稳定的还是短暂的。
借助所有这些数据,他们可以识别出隐藏的或短暂的蛋白质口袋,这些口袋似乎可以稳定所需的蛋白质,以便通过其内部虚拟文库Orchard.ai进行筛选,Orchard.ai主要由他们针对GPCR亚家族开发的模型衍生出的新型化合物组成。为了选择和优先考虑化合物,Deep Apple还创建了一种专有的基于大规模分子对接的评分算法。
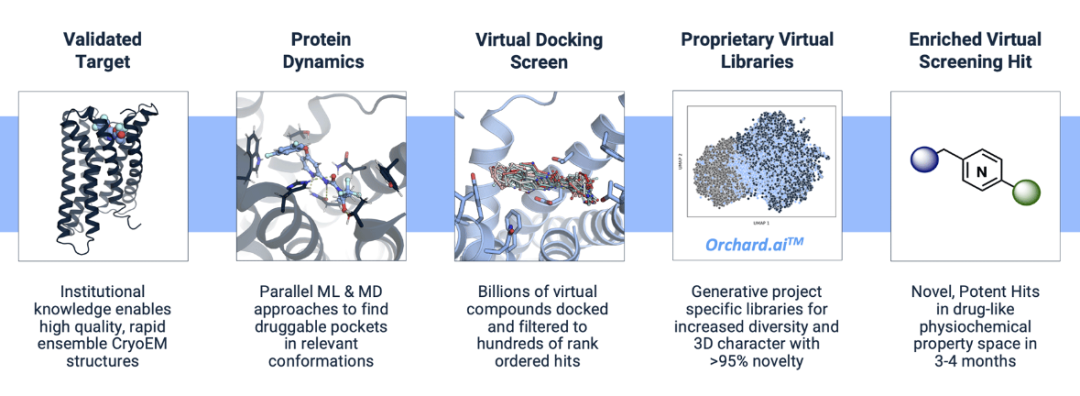
Deep Apple的药物发现引擎平台尽管应用广泛,但该平台最适合针对任何完整的膜蛋白,包括受体蛋白、转运蛋白和离子通道蛋白。Deep Apple专注于GPCR(G蛋白偶联受体),一方面是因为其科学创始人的专业知识,另一方面是因为GPCR的成药机会大。
G蛋白偶联受体(GPCR)是细胞表面受体的最大家族,在生物学中发挥着无处不在的细胞信号作用。事实上,FDA批准上市的药物中有大约三分之一是靶向GPCR。然而,这些药物仅针对GPCR家族蛋白质400多个成员中的100个左右。因此,大多数GPCR代表着大量潜在药物开发靶点,在人类疾病中具有新兴和未开发的作用。
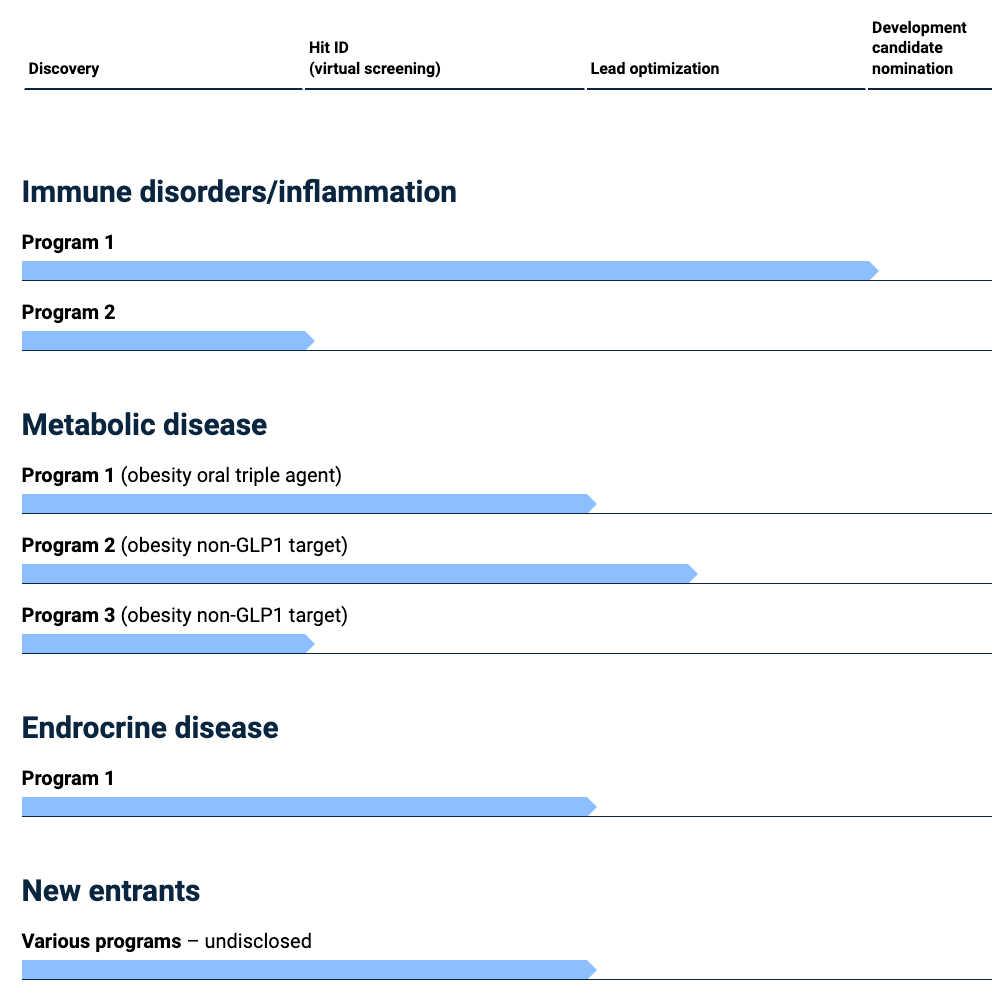
目前,Deep Apple正在推进多个专注于GPCR调节剂的研发项目,这是一个已证明在代谢障碍、炎症、免疫学和内分泌疾病中应用的靶标类别。目前的7个研发管线还都处于早期药物发现阶段,包括几个减肥相关的项目,有望在2024年第二季度提交首个针对炎症目标的药物的临床试验申请,并有希望在2025年初推进更多项目进入临床阶段。
声明:本网站所有内容来源注明为“新医事”,版权均属于新医学事所有,未经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“新医事”。本网注明来源为其他媒体的内容为转载,或系自媒体发布的内容,仅系出于传递更多信息之目的,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。






